Rã-arborícola-de-white | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Estado de conservação | |||||||||||||||
 Pouco preocupante | |||||||||||||||
| Classificação científica | |||||||||||||||
| |||||||||||||||
| Nome binomial | |||||||||||||||
| Litoria caerulea (White, 1790) | |||||||||||||||
| Distribuição geográfica | |||||||||||||||
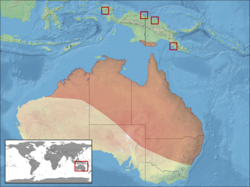 | |||||||||||||||
| Sinónimos | |||||||||||||||
| Rana caerulea (White 1790) Rana austrasiae (Schneider 1799) | |||||||||||||||
A rã-arborícola-de-white,[1] também conhecida como rela-verde-australiana ou simplesmente rela-verde (Litoria caerulea) é uma espécie de rela natural da Austrália e Nova Guiné, com populações introduzidas na Nova Zelândia e Estados Unidos. A espécie pertence ao género Litoria. Fisiologicamente, é muito semelhante a outras espécies do género, especialmente à Litoria splendida e à Litoria infrafrenata.
A rela-verde é uma espécie grande comparada com a maioria das rãs australianas, chegando aos 10 cm de comprimento. A esperança média de vida desta rã em cativeiro, de cerca de dezasseis anos, é longa comparada com a da maioria das rãs. São animais dóceis e bem adaptados para viver perto de áreas ocupadas pelo homem. É comum encontrá-las empoleiradas em janelas ou dentro das casas, comendo insectos que foram atraídos pela luz.
Devido às suas características físicas e comportamentais, a rela-verde tornou-se uma das espécies mais emblemáticas da região, e é popular como animal de estimação exótico no mundo inteiro. As secreções cutâneas desta espécie tem propriedades antibacteriana e antiviral, o que pode ser útil em preparações farmacêuticas.
Classificação

A perereca verde australiana é um membro da família Hylidae e é colocada na subfamília Pelodryadinae, que é endêmica da Austrália e Nova Guiné e inclui mais de 100 espécies nos gêneros Ranoidea e Nyctimystes.[2] O nome comum da espécie, "rã arborícola de White", é uma homenagem à primeira descrição de John White em 1790.[3][4] A perereca verde foi a primeira rã australiana a ser descrita cientificamente; o espécime original encontrou seu caminho para a coleção de Sir Joseph Banks, mas foi destruído quando o Hunterian Museum no Royal College of Surgeons em Londres foi bombardeado na Segunda Guerra Mundial.[5]
A espécie foi originalmente chamada de "rã azul" ( Rana caerulea ), apesar de sua cor verde. Os espécimes que White enviou para a Inglaterra foram danificados pelo conservante e pareciam azuis.[3] A cor do sapo é causada por pigmentos azuis e verdes cobertos por uma camada amarela; o conservante destruiu a camada amarela e deixou o sapo com uma aparência azul. O epíteto específico, caerulea, que em latim significa azul, permaneceu.[6] Este sapo é por vezes referido como Pelodryas caerulea na literatura científica.[6]
Um estudo de 2020 mostrou que Litoria caerulea é na verdade um complexo de espécies que inclui espécies recentemente identificadas, como Litoria mira, que é endêmica da Nova Guiné.[7]
Descrição

A perereca verde é uma perereca gorda e bastante grande e pode crescer até 11,5 cm de comprimento, com as fêmeas totalmente crescidas sendo ligeiramente maiores que os machos. Uma crista gordurosa distinta é vista sobre o olho, e a glândula parotóide é moderadamente grande. A íris é dourada e tem uma pupila cortada horizontalmente, e o tímpano (uma membrana da pele semelhante a um tímpano ) é visível logo atrás do olho. Os membros são curtos e robustos, e grandes discos adesivos estão no final dos dedos que fornecem aderência durante a escalada. Os dedos são cerca de um terço palmados e os dedos dos pés quase três quartos palmados. A cor dorsal depende da temperatura e da natureza do ambiente, variando de marrom ou verde acinzentado a verde esmeralda brilhante. O sapo ocasionalmente tem pequenas manchas brancas de formato irregular nas costas. Os machos têm um saco vocal acinzentado e enrugado sob a garganta, enquanto a garganta das fêmeas é branca. A superfície ventral em ambos os sexos é branco-creme e de textura áspera.[3][8]
Esta rã é semelhante em aparência à magnífica perereca ( R. esplêndida ), que habita apenas o noroeste da Austrália. Os membros mais velhos dessa espécie têm glândulas parotóides muito grandes, que cobrem todo o topo de suas cabeças e se inclinam sobre seus tímpanos. A glândula parotóide da perereca verde é muito menor e também não possui manchas amarelas nas costas e marcas amarelas na mão, virilha e coxa.[9] Pode ser distinguida da perereca de lábios brancos (perereca gigante N. infrafrenatus ) pela distinta faixa branca que a espécie possui ao longo da borda da mandíbula inferior e se estendendo até o ombro, que não está presente na perereca verde.[10]
Algumas rãs hilídeos arborícolas, por exemplo, a perereca verde australiana ( Litoria caerulea ), se beneficiam de dois processos de hidratação ativados higroscopicamente; absorção transcutânea de condensação na pele e redução da perda de água por evaporação. Seu comportamento de limpeza espalha secreções higroscópicas da glândula parotóide em sua pele, facilitando ambos os métodos.[11]

A aparência dos girinos muda ao longo do seu desenvolvimento. Quando recém-nascidos, eles são 8 mm de comprimento e quando totalmente desenvolvido, 44 mm. Eles são inicialmente manchados de marrom e aumentam a pigmentação (para verde ou marrom) durante o desenvolvimento. Suas partes inferiores são inicialmente escuras, mas depois se tornam mais claras. Os ovos são marrons e envoltos em uma gelatina transparente de 1,1 a 1,4 mm de diâmetro.[6]
A chamada é um brawk-brawk-brawk baixo e lento, repetido muitas vezes. Durante a maior parte do ano, as rãs vocalizam de posições altas, como árvores e sarjetas, mas durante a época de reprodução descem para perto de lagoas e poças, onde se reproduzem. Como muitos sapos, as pererecas verdes chamam não apenas para atrair um parceiro, mas também para anunciar sua localização fora da época de acasalamento. Eles são particularmente vocais depois da chuva, mas as razões para isso não são claras. Eles emitem uma chamada de estresse quando estão em perigo, como quando são atacados por um predador ou quando uma pessoa pisa no tronco em que está escondida.[8]
Distribuição e habitat

A perereca verde é nativa das regiões norte e leste da Austrália e das terras baixas da Nova Guiné. A distribuição é limitada principalmente a áreas com climas tropicais quentes e úmidos. Seu alcance vai de Irian Jaya a Port Moresby, e é mais abundante na ilha de Daru. A IUCN sugere "locais dispersos" na Nova Guiné e na Indonésia. Na Austrália, seu alcance se estende desde a região de Kimberley, na Austrália Ocidental, passando pelo Território do Norte e Queensland, até o norte e o centro de Nova Gales do Sul e o extremo nordeste da Austrália Meridional. Sua extensão total de ocupação do solo é de cerca de 4,078,600 quilômetros quadrados.[12]
A espécie foi introduzida nos Estados Unidos e na Nova Zelândia. Nos Estados Unidos, está restrito a duas regiões da Flórida, onde possivelmente foi introduzido por meio do comércio de animais de estimação. Apenas pequenas populações foram encontradas lá, e se eles causaram algum dano ecológico como uma espécie invasora é desconhecido.[13] Na Nova Zelândia, vários indivíduos foram libertados em vários locais em 1897 e 1899, e uma nova introdução acidental foi feita na década de 1940. Nenhum avistamento foi relatado desta espécie desde a década de 1950.[14]
Dependendo de sua localização, as pererecas verdes ocupam vários habitats. Eles preferem florestas úmidas, mas não estão estritamente limitados a florestas tropicais.[8] Eles são freqüentemente encontrados na copa das árvores perto de corpos d'água, mas também ocupam habitats terrestres bem longe da água. Preferem povoamentos antigos de eucalipto, onde as árvores têm cavidades nas quais a água se acumula. Eles são comuns ao longo de cursos de água interiores e podem sobreviver em pântanos (entre os juncos) ou em pastagens em climas mais frios.[10]
As pererecas verdes são pouco incomodadas pela presença de humanos e muitas vezes vivem em estreita associação com eles. Às vezes, eles se perdem dentro das casas e são encontrados em locais como pias e banheiros. Eles também podem ser encontrados em parapeitos externos à noite, comendo insetos atraídos pela luz, e podem se reunir sob iluminação externa pelo mesmo motivo.[3][10] Às vezes ocupam tanques (cisternas), downpipes (calhas) e calhas, pois estes possuem alta umidade e costumam ser mais frios que o ambiente externo. Eles podem ser atraídos para os canos de descarga e tanques durante a época de acasalamento porque os acessórios amplificam suas chamadas.[8] As pererecas verdes parecem ter habilidades de homing, sendo capazes de retornar aos locais de onde foram capturadas a uma distância considerável após serem deslocadas.[5]
Ecologia e comportamento

As pererecas verdes australianas são muito dóceis e não têm medo dos humanos.[8] Elas são noturnas e saem no início da noite para chamar (na primavera e no verão) e caçar comida.[3] Durante o dia, eles encontram áreas frescas, escuras e úmidas, como buracos de árvores ou fendas nas rochas, para dormir. Eles não são uma espécie de floresta tropical, mas aproveitam a chuva que cai quase diariamente e se acumula nas folhas e nas fendas, para se manterem úmidos. Sua pele exala uma camada de cera que ajuda a prevenir a evaporação. Em períodos secos, eles evitam a dessecação escondendo-se em um local fresco, talvez escavando, e envolvendo-se em um casulo feito de pele e muco.[8]
A dieta da perereca verde consiste principalmente de insetos como mariposas, baratas e gafanhotos. Eles também comem aranhas e podem incluir sapos menores e até pequenos mamíferos (incluindo morcegos[15]) entre suas presas.[6][8] Muitos sapos jogam suas línguas pegajosas para a presa e a vítima gruda na ponta e é puxada de volta para a boca e consumida. Uma perereca verde usa essa técnica para presas menores; para itens maiores, no entanto, ele ataca e empurra a presa para dentro da boca com as mãos.[5]
A rã possui alguns predadores nativos, entre eles cobras e pássaros. Desde a colonização europeia da Austrália, predadores não nativos foram introduzidos, principalmente cães e gatos.[16] A espécie tem uma expectativa média de vida em cativeiro de 16 anos, mas alguns vivem mais de 20 anos.[8]
A reprodução ocorre entre novembro e fevereiro.[12] Durante a época de acasalamento, os machos chamam de posições ligeiramente elevadas perto das fontes de água parada em que escolhem se reproduzir.[8]
Como animais de estimação

A perereca verde é uma das rãs de estimação mais populares em todo o mundo. Sua natureza dócil e longa expectativa de vida o tornam uma escolha atraente para donos de animais exóticos. É também uma das rãs mais fáceis de manter; sua dieta é ampla e tem uma forte resistência a doenças. Um problema comumente associado à manutenção dessa espécie como animal de estimação é a superalimentação; as pererecas verdes tendem a se tornar obesas se forem superalimentadas. Na natureza, o esforço de energia é necessário para um sapo capturar sua presa. No entanto, em cativeiro, eles geralmente recebem alimentação viva em um espaço confinado. Isso diminui a atividade necessária para a alimentação, resultando em ganho de peso. Um membro da espécie com excesso de peso deposita camadas de gordura no topo da cabeça e do corpo, dando-lhe uma aparência "atarracada", daí o nome "rã atarracada".[8][17]
Os vaga-lumes rover do gênero Photinus (incluindo o vaga-lume oriental comum da América do Norte) são venenosos para esses sapos, e um incidente foi relatado no qual um vaga-lume foi alimentado com uma perereca verde, que posteriormente morreu.[18]
Conservação

A lei australiana dá status de proteção à perereca verde - junto com toda a fauna australiana - sob a Lei Federal de Proteção Ambiental e Conservação da Biodiversidade de 1999.[19] A União Internacional para a Conservação da Natureza lista o estado de conservação da rã-arborícola-verde como sendo de "menos preocupação", dada a sua ampla distribuição, a sua grande população total e a sua tolerância a uma variedade de tipos de habitat. A tendência da população parece ser estável, e qualquer declínio nos números provavelmente não será rápido o suficiente para justificar listá-lo em uma categoria mais ameaçada.[20]
Em áreas suburbanas, esse sapo é ameaçado pela poluição e pela predação de animais domésticos. Além disso, algumas das rãs foram infectadas com o fungo quitrídio, que causa a doença fatal dos anfíbios, a quitridiomicose. O status do sapo na Nova Guiné é pouco estudado, mas em 2002, cerca de 75.000 indivíduos foram exportados da Indonésia como parte do comércio de animais de estimação, e isso pode afetar as populações em alguns locais. O sapo está presente em várias áreas protegidas na Nova Guiné e foi criado com sucesso em alguns zoológicos australianos. No geral, a principal ameaça a esta espécie é o potencial para uma epidemia de doença generalizada.[20]
Uso em pesquisa
Embora as rãs tenham pulmões, elas absorvem oxigênio pela pele; para que isso ocorra de forma eficiente, a pele deve estar úmida. Uma desvantagem da pele úmida é que patógenos como fungos e bactérias podem prosperar nela, aumentando a chance de infecção. Para neutralizar isso, os sapos secretam peptídeos que destroem esses patógenos. A secreção da glândula paratóide da perereca verde contém 25 caerinas, um grupo de peptídeos com propriedades antibacterianas e antivirais. Os caerins produzidos por rãs desta espécie de diferentes localidades geográficas apresentam diferenças sutis, mas reprodutíveis.[4] As secreções também contêm ceruleínas, que têm os mesmos efeitos fisiológicos do CCK-8, um hormônio digestivo e supressor da fome.[21] Essas ceruleínas agora têm várias aplicações clínicas.[5] Descobriu-se que vários peptídeos das secreções da pele da perereca verde destroem o HIV sem prejudicar as células T saudáveis.[22][23][24]
O fungo Batrachochytrium dendrobatidis, o agente causal da quitridiomicose, está causando declínio em muitas espécies de anfíbios, mas as secreções produzidas pela perereca verde e algumas outras espécies australianas de rã (Litoria chloris e Litoria genimaculata) são protetoras contra esse fungo. Os peptídeos inibem o crescimento do fungo in vitro e acredita-se que essas espécies de sapos não estejam em declínio.[25]
Às vezes, as pererecas verdes são usadas como animais modelo em pesquisas.[26] A estrutura de suas patas foi usada para investigar a microestrutura e as propriedades do epitélio que permite aos animais aderirem a superfícies molhadas.[27]
Notas e referências
- «Australiano flagra rã tentando devorar píton de cerca de 50 cm». G1. Consultado em 20 de agosto de 2023
- «Hylidae». AmphibiaWeb. Consultado em 5 de abril de 2015
- Egerton, p. 383.
- White, John (1790). Journal of a Voyage to New South Wales with sixty-five plates of non descript animals, birds, lizards, serpents, curious cones of trees and other natural productions. Londres: J. Debrett. Consultado em 23 de novembro de 2013. Cópia arquivada em 7 de março de 2019
- Tyler, Michael J; Davies, Margaret (1993). «Family Hylidae» (PDF). Fauna of Australia. Department of the Environment, Water, Heritage and the Arts. Consultado em 4 de abril de 2015
- Bruin, T. (2000). «Litoria caerulea: Information». Animal Diversity Web (Museum of Zoology, University of Michigan). Consultado em 4 de abril de 2015
- Oliver, Paul M.; Rittmeyer, Eric N.; Torkkola, Janne; Donnellan, Stephen C.; Dahl, Chris; Richards, Stephen J. (2020). «Multiple trans-Torres Strait colonisations by tree frogs in the Litoria caerulea group, with the description of a new species from New Guinea». Australian Journal of Zoology. 68 (1). 25 páginas. ISSN 0004-959X. doi:10.1071/ZO20071
- «Fact Sheet: White's Tree Frog». Smithsonian National Zoological Park. Smithsonian Institution. Consultado em 4 de abril de 2015. Arquivado do original em 16 de dezembro de 2005
- Tyler, M. J.; Davies, M.; Martin, A. A. (1977). «A new species of large green tree frog from northern western Australia». Transactions of the Royal Society of South Australia. 101 (5): 133–138. Consultado em 23 de novembro de 2013
- Vanderduys, Eric (2012). Field Guide to the Frogs of Queensland. [S.l.]: Csiro Publishing. 45 páginas. ISBN 978-0-643-10630-7
- Comanns, Philipp (Maio de 2018). «Passive water collection with the integument: mechanisms and their biomimetic potential». Journal of Experimental Biology. 221 (10). PMID 29789349. doi:10.1242/jeb.153130

- «Litoria caerulea». AmphibiaWeb. Consultado em 4 de abril de 2015
- «Litoria caerulea (White, 1790)». Nonindigenous Aquatic Species. U.S. Geological Survey. 2002. Consultado em 4 de abril de 2015. Arquivado do original em 18 de dezembro de 2007
- «Introduced frogs». New Zealand Frog Research Group. 2006. Consultado em 4 de abril de 2015. Cópia arquivada em 24 de dezembro de 2007
- Mikula, P. 2015: Fish and amphibians as bat predators.
- «Green tree frog». Perth Zoo. 10 de maio de 2013. Consultado em 4 de abril de 2015. Arquivado do original em 1 de julho de 2011
- «White's Tree Frog». Frog World. Consultado em 4 de abril de 2015. Arquivado do original em 8 de maio de 2007
- Knight, Michael; Glor, Richard; Smedley, Scott R.; González, Andrés; Adler, Kraig; Eisner, Thomas (1999). «Firefly Toxicosis in Lizards». Journal of Chemical Ecology. 25 (9): 1981–1986. doi:10.1023/A:1021072303515
- «Environment Protection and Biodiversity Conservation Act 1999». Australian Government. Consultado em 4 de abril de 2015
- Hero, Jean-Marc, ed. (2004). «Litoria caerulea». The IUCN Red List of Threatened Species. doi:10.2305/IUCN.UK.2004.RLTS.T41082A10385007. Consultado em 17 de agosto de 2023
- Salmon, Amanda L.; Johnsen, Anders H.; Bienert, Michael; McMurray, Gordon; Nandha, Kiran A.; Bloom, Steve R.; Shaw, Chris (2000). «Isolation, structural characterization, and bio-activity of a novel neuromedin U analog from the defensive skin secretion of the Australasian tree frog, Litoria caerulea». Journal of Biological Chemistry. 275 (7): 4549–4554. PMID 10671478. doi:10.1074/jbc.275.7.4549

- «Frog secretions block HIV». Vanderbilt University. Consultado em 4 de abril de 2015. Arquivado do original em 27 de novembro de 2005
- Vanderbilt University Medical Center (30 de setembro de 2005). «Frog Peptides Block HIV In Lab Study». ScienceDaily
- VanCompernolle, Scott E.; Taylor, R. Jeffery; Oswald-Richter, Kyra; Jiang, Jiyang; Youree, Bryan E.; Bowie, John H.; Tyler, Michael J.; Conlon, J. Michael; Wade, David (Setembro de 2005). «Antimicrobial Peptides from Amphibian Skin Potently Inhibit Human Immunodeficiency Virus Infection and Transfer of Virus from Dendritic Cells to T Cells». Journal of Virology. 79 (18): 11598–11606. PMC 1212620
 . PMID 16140737. doi:10.1128/JVI.79.18.11598-11606.2005
. PMID 16140737. doi:10.1128/JVI.79.18.11598-11606.2005 - Woodhams, Douglas C.; Rollins-Smith, Louise A.; Carey, Cynthia; Reinert, Laura; Tyler, Michael J.; Alford, Ross A. (2006). «Population trends associated with skin peptide defenses against chytridiomycosis in Australian frogs». Oecologia. 146 (4): 531–540. Bibcode:2006Oecol.146..531W. PMID 16205955. doi:10.1007/s00442-005-0228-8
- Von Esse, F. V.; Wright, K. M. (1974). «Effect of intracoelomic propofol in White's tree frogs, Pelodryas caerulea». Bulletin of the Association of Reptilian and Amphibian Veterinarians. 9 (7–8)
- Scholz, Ingo; Barnes, W. Jon P.; Smith, Joanna M.; Baumgartner, Werner (2009). «Ultrastructure and physical properties of an adhesive surface, the toe pad epithelium of the tree frog, Litoria caerulea White». Journal of Experimental Biology. 212 (2): 155–162. PMC 2720997
 . PMID 19112133. doi:10.1242/jeb.019232
. PMID 19112133. doi:10.1242/jeb.019232
Bibliografia
- Bruin, T. «ADW: Litoria caerulea: Information». Consultado em 12 de Junho de 2005
- Cogger, H.G. (1979). Reptiles & Amphibians of Australia. [S.l.]: A. H. & A.W. REED PTY LTS. ISBN 0-589-50108-9
- Tyler, M. J. (1994). Australian Frogs A Natural History. [S.l.]: Reed Books. ISBN 0-7301-0468-0
- Tyler, M.J. & Davies, M. «Fauna of Australia, 8. Family Hylidae» (PDF). Consultado em 12 de Junho de 2005. Arquivado do original (PDF) em 23 de julho de 2005
- Menzies, J.I. (1976). Handbook of Common New Guinea Frogs. [S.l.]: Wau Ecology Institute

Nenhum comentário:
Postar um comentário