Himantura uarnak | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Estado de conservação | |||||||||||||||||||
 Em perigo (IUCN 3.1) [1] | |||||||||||||||||||
| Classificação científica | |||||||||||||||||||
| |||||||||||||||||||
| Nome binomial | |||||||||||||||||||
| Himantura uarnak (Forsskål, 1775) ou (J. F. Gmelin, 1789) | |||||||||||||||||||
| Distribuição geográfica | |||||||||||||||||||
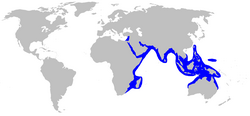 Área de distribuição de Himantura uarnak | |||||||||||||||||||
| Sinónimos | |||||||||||||||||||
| |||||||||||||||||||
Himantura uarnak é uma espécie de arraia da família Dasyatidae. Habita águas costeiras do oeste do oceano Índico, incluindo o mar Vermelho e o mar Arábico; também é uma migrante lessepsiana no Mediterrâneo oriental. É uma espécie de grande porte, alcançando 2 m de largura, com disco de nadadeira peitoral em forma de losango e uma cauda extremamente longa sem dobras de barbatana. Tanto seu nome comum (em inglês: reticulate whipray ou honeycomb stingray) quanto o nome científico fazem referência ao padrão de coloração dorsal ornamentado, com muitos pontos escuros pequenos e próximos ou reticulações sobre um fundo mais claro. No entanto, Himantura uarnak é apenas uma das várias arraias de grande porte com manchas no Indo-Pacífico, o que, aliado à variabilidade de sua coloração com a idade e a localidade, resultou em grande confusão taxonômica.
Frequentemente encontrada descansando no fundo do mar durante o dia, Himantura uarnak é uma predadora de organismos bentônicos invertebrados e peixes ósseos. Como outras arraias, é ovovivípara, com os embriões em desenvolvimento nutridos inicialmente por vitelo e, posteriormente, por histotrofo ("leite uterino"). As fêmeas dão à luz ninhadas de até cinco filhotes no verão, após um período de gestação de um ano. Himantura uarnak é pescada em partes do oceano Índico para carne, pele, cartilagem e outros fins. É altamente suscetível à depleção populacional devido ao seu grande tamanho, hábitos costeiros e baixa taxa reprodutiva, além de ser ameaçada pela extensa destruição de habitat. Como resultado, a União Internacional para a Conservação da Natureza (IUCN) classificou esta espécie como em perigo.[1]
Taxonomia e filogenia
Em 1775, Carsten Niebuhr publicou Descriptiones animalium – avium, amphibiorum, piscium, insectorum, vermium: quæ in itinere orientali observavit, obra de seu falecido amigo, o naturalista sueco Pehr Forsskål. Nela, Forsskål descreveu Raja sephen, agora conhecida como raia-cauda-de-vaca, com uma variante manchada chamada uarnak ورنك, nome árabe para arraias nas costas do mar Vermelho. Nenhum espécime-tipo foi designado.[2] A descrição de Forsskål serviu de base para duas publicações subsequentes que nomearam a arraia manchada como uma espécie distinta: Raia scherit de Pierre-Joseph Bonnaterre em 1788 e Raja uarnak de Johann Friedrich Gmelin em 1789. Embora o nome de Bonnaterre tenha sido publicado primeiro e, portanto, tivesse precedência, autoridades posteriores consideraram uarnak de Forsskål como o nome disponível mais antigo, mesmo não fazendo parte de uma nomenclatura binomial inicialmente. Assim, fontes modernas adotam uarnak como o epíteto específico válido, atribuindo a autoria a Gmelin ou Forsskål.[3][4] Em 1837, Johannes Peter Müller e Friedrich Gustav Jakob Henle incluíram Himantura uarnak no gênero recém-criado Himantura; David Starr Jordan e Barton Warren Evermann a designaram como a espécie-tipo em 1896.[5]
Himantura uarnak é estreitamente relacionada a H. undulata [en], H. leoparda [en], bem como a espécie recentemente descrita H. tutul (anteriormente confundida com H. leoparda)[6] e H. australis [en]. Todas as cinco espécies são muito semelhantes em tamanho e forma, e seus padrões de coloração podem se sobrepor em certa medida,[7] resultando em uma longa história de confusão taxonômica que só recentemente começou a ser esclarecida.[8] Em 2004, Mabel Manjaji designou como complexo de espécies "uarnak" um grupo de espécies geneticamente não relacionadas, incluindo H. fai, H. gerrardi, H. jenkinsii, H. leoparda, H. toshi, H. uarnak e H. undulata, além de três espécies ainda não descritas.[9] Embora as espécies desse complexo possam habitar áreas geográficas e habitats sobrepostos, a probabilidade de hibridização entre elas é rara.[10] A melhor abordagem para identificar indivíduos nesse complexo é o uso do código de barras COI universal.[10]
Mais recentemente, os gêneros da família de arraias Dasyatidae foram redefinidos com base em filogenética molecular. Espécies anteriormente classificadas como Himantura agora pertencem a gêneros distintos.[11] A própria arraia Himantura uarnak varia em aparência ao longo de sua distribuição, e comparações taxonômicas adicionais são necessárias para determinar se suas morfologias de cor manchadas e reticuladas representam, de fato, espécies diferentes.[1] Nomes comuns alternativos em inglês para esta arraia incluem honeycomb ray, coachwhip ray, leopard stingray, longtail stingray e marbled stingray; alguns desses nomes são compartilhados por outras espécies semelhantes.[3]
Descrição

O disco de nadadeira peitoral é em forma de losango, mais largo que longo, com margens anteriores quase retas e o focinho e cantos externos quadrangulares. O ápice da nadadeira peitoral é estreitamente arredondado, com a margem anterior quase reta.[12] Em filhotes, o disco é tão largo quanto longo, com um focinho mais obtuso e cantos arredondados.
Os olhos são pequenos e possuem um diâmetro interorbital reduzido.[12] Imediatamente após os olhos, encontram-se os espiráculos, que são aberturas respiratórias pareadas. Uma cortina de pele curta e larga, com margem posterior minuciosamente franjada, está presente entre as narinas longas e finas. A boca é relativamente pequena, com uma concavidade profunda no centro da mandíbula inferior e sulcos rasos nos cantos, estendendo-se até a mandíbula inferior.[13] Uma fileira de 4 a 5 papilas (estruturas semelhantes a mamilos) está presente no assoalho da boca. Há 26–40 fileiras de dentes superiores e 27–44 fileiras de dentes inferiores.[14] As nadadeiras pélvicas são pequenas e triangulares. A cauda é semelhante a um chicote, extremamente fina, medindo 3 a 3,5 vezes o comprimento do disco quando intacta, e não possui dobras de barbatana. Geralmente, um espinho serrilhado está localizado na superfície superior da cauda, a alguma distância da base.[13]
Arraias adultas possuem uma ampla faixa de dentículos dérmicos achatados em forma de coração, que se estendem do espaço entre os olhos até o espinho da cauda, aumentando em densidade com a idade, juntamente com dois espinhos perolados grandes no centro das costas. A cauda após o espinho é coberta por pequenos espinhos. A faixa dorsal de dentículos está amplamente desenvolvida quando os filhotes atingem 50 cm de largura. A coloração de Himantura uarnak varia substancialmente com a idade e a localidade. Adultos geralmente apresentam um padrão dorsal de numerosos pontos marrons escuros ou reticulações bem espaçados sobre um fundo bege a marrom-amarelado, que se torna enegrecido após o espinho com faixas mais claras nas laterais. Essa coloração texturizada é frequentemente descrita como um “padrão de colmeia” e é um exemplo clássico de uma célula de Voronoi, que surge frequentemente na natureza com arranjos repetidos de estruturas poligonais.[15] Esse padrão é uma otimização evolutiva que minimiza a energia de construção do padrão, além de proporcionar coloração críptica.[15] A face ventral é pálida, de cor branca, sem marcações. Filhotes são amarelados na parte superior com pontos escuros minúsculos e densamente agrupados, cerca de sete pontos em uma linha entre os espiráculos e três fileiras de pontos à frente do espinho.[13] Esses pontos tendem a ser maiores em filhotes e diminuem de tamanho à medida que o indivíduo envelhece, formando o padrão distinto de “colmeia/leopardo”, considerado um padrão de crescimento alométrico negativo.[16]

Esta espécie de grande porte foi relatada como alcançando uma largura de disco de 2 m, um comprimento total de 6 m e um peso de 120 kg.[3][14]
Distribuição e habitat

O habitat de Himantura uarnak inclui recifes de coral, águas salobras e ambientes marinhos. Nesses ecossistemas, ela pode ser encontrada em áreas costeiras e em substratos moles.[12] Sua distribuição ocorre no norte de Taiwan, no oeste do oceano Índico (principalmente na Malásia, Myanmar, Indo-Pacífico), no mar Vermelho, a oeste até Natal, na África do Sul, e no mar Arábico.[8][12] Há 30 anos, ela entrou no mar Mediterrâneo através do Canal de Suez e agora é comum no sudeste do Mediterrâneo.[17] A recentemente descrita H. australis, anteriormente confundida com H. uarnak, parece ser comum apenas em águas australianas, onde ocorre da baía Shark a Brisbane.[1][13]
De natureza bentônica, Himantura uarnak é geralmente encontrada sobre planícies arenosas perto de praias, em lagunas e ao redor de recifes de coral, desde a zona entremarés até águas offshore com 50 m de profundidade ou mais.[1] Esses microhabitats (planícies de areia entremarés, planícies de areia rasas e leitos de ervas marinhas) são utilizados de forma diferente entre as estações quentes e frias.[18] Na baía Shark, ela frequenta planícies de areia entremarés durante a estação quente e se desloca para leitos de erva marinha ligeiramente mais profundos na estação fria.[19] Esta espécie é tolerante a baixas salinidades e é conhecida por entrar em estuários e manguezais,[20] embora registros em água doce no Sudeste Asiático não sejam verificados e podem representar identificações errôneas.[21] Suas temperaturas de água preferidas estão entre 23 e 26 °C.[22]
Biologia e ecologia

Durante o dia, Himantura uarnak é geralmente inativa e passa muito tempo descansando imóvel no fundo do mar, às vezes enterrada na areia.[20] Na baía Shark, Austrália Ocidental, essa arraia pode ser encontrada descansando sozinha ou em pequenos grupos em águas muito rasas durante a maré alta. A vida em condições de luz brilhante e rasa evoluiu a visão da arraia para se especializar em visão fotópica.[23] Esses olhos possuem uma concentração de células ganglionares, cones e poder de resolução espacial que indicam visão de cores e especialização horizontal alongada da acuidade visual.[23]

Uma linha lateral está presente na arraia e se estende até a ponta de sua cauda extremamente longa, proporcionando alerta antecipado de predadores que se aproximam, como golfinhos Tursiops aduncus e tubarões da família Sphyrnidae. Alguns encontros extremamente raros documentaram golfinhos sendo feridos, até mortos, por ferimentos causados por espinhos de Himantura uarnak inseridos nas laterais dos golfinhos. Esses encontros são teoricamente mais prováveis em locais de alimentação em águas rasas onde Himantura uarnak tende a residir.[24] A gravidade da reação aos ferimentos por espinhos não é considerada correlacionada à idade ou tamanho da arraia.[24] À medida que as arraias envelhecem, há maior chance de perda das glândulas de veneno e da bainha protetora do espinho.[25] A raia-cauda-de-vaca (Pastinachus sephen) prefere descansar com Himantura uarnak em vez de outras de sua própria espécie, porque as caudas mais longas de Himantura uarnak proporcionam uma detecção superior de predadores. Esses grupos de espécies mistas frequentemente se organizam em uma "roseta", com suas caudas apontando radialmente para fora para máxima consciência de predadores.[26]
Himantura uarnak preda uma variedade de organismos bentônicos e neríticos, incluindo caranguejos, camarões, tamarutacas, bivalves, gastrópodes, vermes, águas-vivas e peixes ósseos.[3][27] No oeste do oceano Índico, cerca de dois terços de sua dieta consistem em peixes, em particular peixes da família Leiognathidae e engraulídeos, com camarões e outros crustáceos compondo a maior parte do restante.[28] Em contrapartida, as arraias em águas australianas aparentemente não são ictiófagas e são conhecidas por consumir camarões da família Penaeidae.[29] Himantura uarnak desempenha um papel ecológico importante como mesopredadora e exerce um forte impacto de cima para baixo em ambientes costeiros na ausência de distúrbios humanos.[30] Predadores bentônicos, incluindo Himantura uarnak, estão associados a cascatas tróficas que resultam em maior densidade populacional de arraias quando ocorre sobrepesca de predadores terciários (principalmente tubarões).[31]
Os parasitas conhecidos desta espécie incluem Anthrobothrium loculatum,[32] Dendromonocotyle colorni,[33] Halysiorhynchus macrocephalus,[34] Monocotyle helicophallus, M. multiparous e M. spiremae,[35] Thaumatocotyle australensis,[36] e Tylocephalum chiralensis.[37] Uma bactéria marinha, Vibrio alginolyticus, foi documentada infectando Himantura uarnak, causando letargia, lesões cutâneas necróticas esbranquiçadas e úlceras na pele, e pode ser tratada com amicacina para prevenir a mortalidade.[38]
Como outras arraias, Himantura uarnak é ovovivípara: os embriões em desenvolvimento são inicialmente sustentados por vitelo, que é posteriormente substituído por histotrofo ("leite uterino", enriquecido com proteínas e lipídios) produzido pela mãe.[1] As fêmeas dão à luz até cinco filhotes no verão, após um período de gestação de um ano.[27] Na África do Sul, os recém-nascidos medem 28–30 cm de largura, e a maturação sexual é alcançada com uma largura de disco de aproximadamente 1 m, correspondendo a uma idade de 4 a 5 anos.[39] Na Austrália, os recém-nascidos medem 21–28 cm de largura, com machos relatados como atingindo a maturidade com 82–84 cm de largura.[13] Os filhotes de H. leoparda e H. undulata diferem em tamanho ao nascer, forma do disco, desenvolvimento de dentículos e quantidade de manchas, sendo, de fato, mais distintos entre si do que os adultos das espécies de Himantura.[9] A baía Shark pode servir como uma área de berçário para arraias jovens.[19] Embora as espécies no complexo de espécies "uarnak" pareçam morfologicamente e fisiologicamente semelhantes, a hibridização interespecífica ainda não foi claramente documentada a partir de marcadores genéticos nucleares.[10] É possível que diferenças interespecíficas no seio urogenital das fêmeas e na extensão e forma distal do clásper dos machos resultem em isolamento reprodutivo.[10]
Interações humanas

Himantura uarnak luta fortemente quando capturada com anzol e linha, sendo, portanto, popular entre pescadores desportivos, que geralmente a liberam viva.[39] Esta espécie é capturada por intensas pescas artesanais e comerciais em partes do oeste do oceano Índico, usando redes de arrasto, redes de emalhar e redes de encalhe, redes de cerco e palangres.[1] Pescarias na costa do Paquistão documentaram a captura de Himantura uarnak, com um estudo indicando que, de 1977 a 2019, aproximadamente mais de 2.840 toneladas do complexo "uarnak" foram capturadas como subproduto das pescarias.[40] O ano de 1982 foi documentado como o auge da pesca comercial de arraias, com mais de 49.017 toneladas de arraias capturadas e vendidas.[40] A temporada de pico para captura de Himantura uarnak ocorre de maio a agosto.[40] As arraias capturadas comercialmente são frequentemente usadas como matéria-prima para produzir farinha de peixe para a indústria avícola, com algumas das “asas” sendo exportadas para a Malásia e a Tailândia.[40]
A carne, a pele e a cartilagem são utilizadas, embora esta espécie não seja um peixe alimentar altamente valorizado. Ela também tem aplicações na medicina tradicional chinesa, e sua cauda costuma ser vendida.[3] A medicina tradicional na Índia usava Himantura uarnak como lactogogos, onde o consumo da carne era encontrado para aumentar a produção de leite em novas mães, particularmente entre as camadas mais pobres da sociedade.[41] Além disso, Himantura uarnak foram usadas para tratar disenteria, respiração ofegante e bronquite no estado de Tâmil Nadu, principalmente por comunidades costeiras e tribais no sul da Ásia e em Myanmar.[41][42]
A União Internacional para a Conservação da Natureza (IUCN) classificou Himantura uarnak como em perigo. Seu grande tamanho, preferências por habitats costeiros e baixa taxa reprodutiva a tornam suscetível à pesca predatória. Embora faltem dados específicos, declínios significativos nas capturas gerais de arraias foram documentados dentro de sua área de distribuição. Dados não específicos de arraias na Malásia e na Indonésia estimam que populações localizadas reduziram de 50 a 99% nas últimas três gerações.[43] Globalmente, as populações são suspeitas de terem reduzido de 50 a 75% nos últimos 75 anos.[43] A destruição de habitat também ameaça esta espécie, enquanto a poluição da água e práticas de pesca destrutivas também podem ter contribuído para seu declínio.
Himantura uarnak é ocasionalmente oferecida no comércio de aquários domésticos, mas deve ser evitada devido às suas proporções massivas.[44] Também é mantida em alguns aquários públicos, como o Aquário do Pacífico (onde é um dos maiores habitantes do aquário),[45] o aquário do hotel Atlantis Dubai e o Aquário Steinhart da Academia de Ciências da Califórnia.[46]
Conservação
O estado de espécie em perigo da IUCN para Himantura uarnak levou a crescentes preocupações com a segurança da população global. Pesquisas recentes destacaram a necessidade de conservar ambientes de lagunas que mantenham o fluxo hidrológico desimpedido de água de maré.[47] Proteger manguezais saudáveis, leitos de ervas marinhas e habitats de planícies de lama garante segurança alimentar e refúgios para megafauna, incluindo Himantura uarnak.[47] Além disso, corredores de movimento precisam ser priorizados para garantir a conectividade entre locais de forrageamento e habitats de filhotes e adultos.[47] A concepção e implementação de Áreas Marinhas Protegidas é um dos primeiros passos fundamentais para garantir um habitat seguro para as arraias. A integração de técnicas como análises de DNA ambiental pode ser usada para monitorar eficazmente populações localizadas e seus habitats críticos.[48]
Referências
- Sherman, C.S., Bin Ali, A., Bineesh, K.K., Derrick, D., Dharmadi, Fahmi, Fernando, D., Haque, A.B., Maung, A., Seyha, L., Tanay, D., Utzurrum, J.A.T., Vo, V.Q. & Yuneni, R.R. (2021). «Himantura uarnak». IUCN. Lista Vermelha de Espécies Ameaçadas. 2021: e.T201098826A124528737. doi:10.2305/IUCN.UK.2021-2.RLTS.T201098826A124528737.en
 . Consultado em 30 de junho de 2025
. Consultado em 30 de junho de 2025 - Forsskål, P.S. (1775). Niebuhr, C, ed. Descriptiones animalium – avium, amphibiorum, piscium, insectorum, vermium: quæ in itinere orientali observavit Petrus Forskål (post mortem auctoris edidit Carsten Niebuhr). Adjuncta est materia medica kahirina atque tabula maris Rubri geographica. [S.l.]: ex officina Mölleri, Hauniae. pp. 17–18. Consultado em 30 de junho de 2025
- Froese, Rainer; Pauly, Daniel (eds.) (2009). "Himantura uarnak" em FishBase. Versão março 2009.
- «Himantura uarnak». GBIF
- Jordan, D.S.; B.W. Evermann (3 de outubro de 1896). «The fishes of North and Middle America: a descriptive catalogue of the species of fish-like vertebrates found in the waters of North America, north of the Isthmus of Panama (Part I)». Bulletin of the United States National Museum. 47: 1–1240
- Borsa, P. (2017). «Comment on 'Annotated checklist of the living sharks, batoids and chimaeras (Chondrichthyes) of the world, with a focus on biogeographical diversity' by Weigmann (2016)» (PDF). Journal of Fish Biology. 90 (4): 1170–1175. Bibcode:2017JFBio..90.1170B. PMID 28026866. doi:10.1111/jfb.13235. Consultado em 30 de junho de 2025
- Borsa, P.; Durand, Jean-Dominique; Shen, Kang-Ning; Irma S.Arlyza; Dedy D.Solihin; Berrebi, Patrick (2013). «Himantura tutul sp. nov. (Myliobatoidei: Dasyatidae), a new ocellated whipray from the tropical Indo-West Pacific, described from its cytochrome-oxidase I gene sequence». Comptes Rendus Biologies. 336 (2): 82–92. PMID 23608177. doi:10.1016/j.crvi.2013.01.004. Consultado em 30 de junho de 2025
- Philippe Borsa; Collin T. Williams; Ashlie J. McIvor; Thierry B. Hoareau; Michael L. Berumen (2021). «Neotype designation and re-description of Forsskål's reticulate whipray Himantura uarnak». Marine Biodiversity. 51 (2). 28 páginas. Bibcode:2021MarBd..51...28B. doi:10.1007/s12526-021-01180-1. hdl:10754/665804
 . Consultado em 30 de junho de 2025
. Consultado em 30 de junho de 2025 - Last, P.R.; Manjaji-Matsumoto, B.M. (2008). «Himantura leoparda sp. nov., a new whipray (Myliobatoidei: Dasyatidae) from the Indo–Pacific». In: Last, P.R.; W.T. White; J.J. Pogonoski. Descriptions of New Australian Chondrichthyans. [S.l.]: CSIRO Marine and Atmospheric Research. pp. 292–302. ISBN 978-0-1921424-1-2
- Arlyza, I. S.; Shen, K. -N.; Solihin, D. D.; Soedharma, D.; Berrebi, P.; Borsa, P. (1 de janeiro de 2013). «Species boundaries in the Himantura uarnak species complex (Myliobatiformes: Dasyatidae)». Molecular Phylogenetics and Evolution. 66 (1): 429–435. Bibcode:2013MolPE..66..429A. ISSN 1055-7903. PMID 23023209. doi:10.1016/j.ympev.2012.09.023. Consultado em 30 de junho de 2025
- Last, P.R.; Naylor, G.J.; Manjaji-Matsumoto, B.M. (2016). «A revised classification of the family Dasyatidae (Chondrichthyes: Myliobatiformes) based on new morphological and molecular insights». Zootaxa. 4139 (3): 345–368. PMID 27470808. doi:10.11646/zootaxa.4139.3.2
- Tun, Myo Min (2020). «STUDY ON THE FISHERY STATUS OF COACH WHIPRAY, HIMANTURA UARNAK AT TWO FISH LANDING SITES OF MON STATE» (PDF). Myanmar Academy. XVIII (4B): 335–341. Consultado em 30 de junho de 2025
- Last, P.R.; J.D. Stevens (2009). Sharks and Rays of Australia segunda ed. [S.l.]: Harvard University Press. pp. 449–440. ISBN 978-0-674-03411-2
- Smith, J.L.B.; Smith, M.M.; Heemstra, P. (2003). Smiths' Sea Fishes. [S.l.]: Struik. pp. 139–140. ISBN 978-1-86872-890-9
- Perricone, Valentina; Grun, Tobias B.; Rendina, Francesco; Marmo, Francesco; Candia Carnevali, Maria Daniela; Kowalewski, Michal; Facchini, Angelo; De Stefano, Mario; Santella, Luigia; Langella, Carla; Micheletti, Alessandra (agosto de 2022). «Hexagonal Voronoi pattern detected in the microstructural design of the echinoid skeleton». Journal of the Royal Society Interface (em inglês). 19 (193). ISSN 1742-5662. PMC 9363984
 . PMID 35946165. doi:10.1098/rsif.2022.0226
. PMID 35946165. doi:10.1098/rsif.2022.0226 - Arlyza1, Irma; Solihin, Dedy; Soedharma, Dedi (25 de agosto de 2013). «Distribution Patterns of the Morphology, Species, and Sex in the Stingray Species Complex of Himantura uarnak, Himantura undulata, and Himantura leoparda in Indonesia». Makara Journal of Science. 17 (2). ISSN 2356-0851. doi:10.7454/mss.v17i2.2097
 . Consultado em 30 de junho de 2025
. Consultado em 30 de junho de 2025 - Atlas of Exotic Fishes in the Mediterranean Sea (Himantura uarnak) (PDF) 2ª ed. Paris, Monaco: CIESM Publishers. 2021. 366 páginas. Consultado em 30 de junho de 2025
- Vaudo, Jeremy J.; Heithaus, Michael R. (1 de novembro de 2009). «Spatiotemporal variability in a sandflat elasmobranch fauna in Shark Bay, Australia». Marine Biology (em inglês). 156 (12): 2579–2590. Bibcode:2009MarBi.156.2579V. ISSN 1432-1793. doi:10.1007/s00227-009-1282-2. Consultado em 30 de junho de 2025
- Vaudo, J.J.; M.R. Heithaus (2009). «Spatiotemporal variability in a sandflat elasmobranch fauna in Shark Bay, Australia». Marine Biology. 156 (12): 2579–2590. Bibcode:2009MarBi.156.2579V. doi:10.1007/s00227-009-1282-2
- Ferrari, A.; A. Ferrari (2002). Sharks. [S.l.]: Firefly Books. p. 220. ISBN 978-1-55209-629-1. Consultado em 30 de junho de 2025
- Compagno, L.J.V.; T.R. Roberts (1982). «Freshwater stingrays (Dasyatidae) of Southeast Asia and New Guinea, with description of a new species of Himantura and reports of unidentified species». Environmental Biology of Fishes. 7 (4): 321–339. Bibcode:1982EnvBF...7..321C. doi:10.1007/BF00005567
- Last, P.R.; Compagno, L.J.V. (1999). «Myliobatiformes: Dasyatidae». In: Carpenter, K.E.; Niem, V.H. FAO identification guide for fishery purposes. The living marine resources of the Western Central Pacific. Roma: Food and Agricultural Organization of the United Nations. pp. 1479–1505. ISBN 978-92-5-104302-8
- Garza Gisholt, Eduardo (2015). Visual specializations and light detection in Chondrichthyes. [S.l.: s.n.] Consultado em 30 de junho de 2025
- Spanier, Goffman, Kerem, Lavalli, Ehud, Oz, Dan, Kari (2000). «Injury of an Indian Ocean bottlenose dolphin (Tursiops aduncus) in the Red Sea by a stingray spine». Aquatic Mammals. 26 (3): 196–201. Consultado em 30 de junho de 2025 – via Research Gate
- Herald, Earl Stannard (1961). «Living fishes of the world». (No Title). The world of nature series (em inglês). Consultado em 30 de junho de 2025
- Semeniuk, C.A.D.; L.M. Dill (2006). «Anti-Predator Benefits of Mixed-Species Groups of Cowtail Stingrays (Pastinachus sephen) and Whiprays (Himantura uarnak) at Rest». Ethology. 112 (1): 33–43. Bibcode:2006Ethol.112...33S. doi:10.1111/j.1439-0310.2006.01108.x
- Michael, S.W. (1993). Reef Sharks & Rays of the World. [S.l.]: Sea Challengers. p. 87. ISBN 978-0-930118-18-1
- Randall, J.E.; J.P. Hoover (1995). Coastal fishes of Oman. [S.l.]: University of Hawaii Press. p. 46. ISBN 978-0-8248-1808-1
- Salini, J.P.; S.J.M. Blaber; D.T. Brewer (outubro de 1990). «Diets of piscivorous fishes in a tropical Australian estuary, with special reference to predation on penaeid prawns». Marine Biology. 105 (3): 363–374. Bibcode:1990MarBi.105..363S. doi:10.1007/BF01316307
- Vaudo, Jeremy J.; Heithaus, Michael R. (1 de novembro de 2009). «Spatiotemporal variability in a sandflat elasmobranch fauna in Shark Bay, Australia». Marine Biology (em inglês). 156 (12): 2579–2590. Bibcode:2009MarBi.156.2579V. ISSN 1432-1793. doi:10.1007/s00227-009-1282-2. Consultado em 30 de junho de 2025
- Mateos-Molina, Daniel; Bejarano, Ivonne; Pittman, Simon J.; Möller, Mona; Antonopoulou, Marina; Jabado, Rima W. (1 de março de 2024). «Coastal lagoons in the United Arab Emirates serve as critical habitats for globally threatened marine megafauna». Marine Pollution Bulletin. 200. 116117 páginas. Bibcode:2024MarPB.20016117M. ISSN 0025-326X. doi:10.1016/j.marpolbul.2024.116117. Consultado em 30 de junho de 2025
- Vijayalakshmi, C.; S. Sarada (junho de 1993). «Studies on the new species Anthrobothrium loculatum parasite from Dasyatis (Himantura) uarnak (Forskal)». Boletín Chileno de Parasitología. 48 (1–2): 12–16. PMID 8110367
- Chisholm, L.A.; I.D. Whittington; G.C. Kearn (2001). «Dendromonocotyle colorni sp. n. (Monogenea: Monocotylidae) from the skin of Himantura uarnak (Dasyatididae) from Israel and a new host record for D. octodiscus from the Bahamas». Folia Parasitologica. 48 (1): 15–20. PMID 11266131. doi:10.14411/fp.2001.004

- Beveridge, I.; R.A. Campbell (junho de 1992). «Redescription of Halysiorhynchus macrocephalus (Cestoda: Trypanorhyncha), a genus newly recorded from the Australasian region». Systematic Parasitology. 22 (2): 151–157. doi:10.1007/BF00009607
- Measures, L.N.; M. Beverley-Burton; A. Williams (outubro de 1990). «Three new species of Monocotyle (Monogenea: Monocotylidae) from the stingray, Himantura uarnak (Rajiformes: Dasyatidae) from the Great Barrier Reef: phylogenetic reconstruction, systematics and emended diagnoses». International Journal for Parasitology. 20 (6): 755–767. PMID 2242960. doi:10.1016/0020-7519(90)90009-C
- Beverley-Burton, M.; A. Williams (1989). «Merizocotyle icopae, Sp-Nov, and Thaumatocotyle australensis, Sp-Nov, (Monogenea, Monocotylidae) From the Nasal Cavities of Rajiform Elasmobranchs of the Great-Barrier-Reef». Australian Journal of Zoology. 37 (1): 25–35. doi:10.1071/ZO9890025
- Vijayalakshmi, C.; S. Sarada (julho–dezembro de 1995). «Studies on the new species Tylocephalum chiralensis, parasite from Dasyatis (Himantura) uarnak (Förskal) from Chirala coast, Andhra Pradesh, India». Boletín Chileno de Parasitología. 50 (3–4): 73–75. PMID 8762670
- Emam, Arafah M.; Hashem, Mahmoud; Gadallah, Ahmed Omar; Haridy, Mohie (1 de junho de 2019). «An outbreak of Vibrio alginolyticus infection in aquarium-maintained dark-spotted (Himantura uarnak) and Tahitian (H. fai) stingrays». Egyptian Journal of Aquatic Research. 45 (2): 153–158. Bibcode:2019EgJAR..45..153E. ISSN 1687-4285. doi:10.1016/j.ejar.2019.05.003

- Heemstra, E. (2004). Coastal fishes of Southern Africa. [S.l.]: NISC and SAIAB. p. 83. ISBN 978-1-920033-01-9
- Moazzam, Badar-Osmany, Muhammad, Hamid (2021). «SPECIES COMPOSITION, COMMERCIAL LANDINGS, DISTRIBUTION AND CONSERVATION OF STINGRAYS (CLASS PISCES: FAMILY DASYATIDAE) FROM PAKISTAN» (PDF). International Journal of Biology and Biotechnology. 18 (2): 339–363. Consultado em 30 de junho de 2025
- Karnad, Divya; Narayani S; Kottillil, Shruthi; Kottillil, Sudha; Gupta, Trisha; Barnes, Alissa; Dias, Andrew; Krishna, Y. Chaitanya (20 de outubro de 2022). «Shark and ray meat consumption as a threat to India's elasmobranchs» (PDF). Authorea. 1 (1): 1–9. doi:10.22541/au.166603256.66186502/v2. Consultado em 30 de junho de 2025
- Esakkimuthu, S.; Sylvester Darvin, S.; Mutheeswaran, S.; Gabriel Paulraj, M.; Pandikumar, P.; Ignacimuthu, S.; Al-Dhabi, N. A. (28 de junho de 2018). «A study on food-medicine continuum among the non-institutionally trained siddha practitioners of Tiruvallur district, Tamil Nadu, India». Journal of Ethnobiology and Ethnomedicine. 14 (1). 45 páginas. ISSN 1746-4269. PMC 6025710
 . PMID 29954417. doi:10.1186/s13002-018-0240-9
. PMID 29954417. doi:10.1186/s13002-018-0240-9
- «Reticulate Whipray - Himantura uarnak» (em inglês). 16 de fevereiro de 2021. Consultado em 30 de junho de 2025
- «Elasmobranch Enthusiasts (Part 1): Modern Husbandry – Space». Saltwater Smarts. Consultado em 30 de junho de 2025. Cópia arquivada em 14 de janeiro de 2013
- «Online Learning Center». Aquarium of the Pacific. Consultado em 30 de junho de 2025
- «Reef Lagoon Field Guide». California Academy of Sciences in San Francisco, CA. Consultado em 30 de junho de 2025
- Mateos-Molina, Daniel; Bejarano, Ivonne; Pittman, Simon J.; Möller, Mona; Antonopoulou, Marina; Jabado, Rima W. (1 de março de 2024). «Coastal lagoons in the United Arab Emirates serve as critical habitats for globally threatened marine megafauna». Marine Pollution Bulletin. 200. 116117 páginas. Bibcode:2024MarPB.20016117M. ISSN 0025-326X. doi:10.1016/j.marpolbul.2024.116117. Consultado em 30 de junho de 2025
- Castro-Cubillos, Margoth L.; Taylor, Joe D.; Mastretta-Yanes, Alicia; Benítez-Villalobos, Francisco; Islas-Villanueva, Valentina (16 de junho de 2022). «Monitoring of benthic eukaryotic communities in two tropical coastal lagoons through eDNA metabarcoding: a spatial and temporal approximation». Scientific Reports (em inglês). 12 (1). 10089 páginas. Bibcode:2022NatSR..1210089C. ISSN 2045-2322. PMC 9203746
 . PMID 35710829. doi:10.1038/s41598-0
. PMID 35710829. doi:10.1038/s41598-0
